La semana pasada salió publicado un nuevo estudio en la revista científica Journal of Mammalian Evolution sobre los oídos de los roedores endémicos del Caribe* (Da Cunha et al., 2023). Específicamente en este trabajo examinamos en detalle las estructuras del oído interno para determinar si nos pueden ayudar a entender mejor como están relacionadas las distintas especies, con un enfoque particular en las especies gigantes extintas: Amblyrhiza inundata (Anguila, Isla de San Martín y San Bartolomé), Clidomys osborni (Jamaica) y Elasmodontomys obliquus (Puerto Rico). Estas tres especies gigantes generalmente se han clasificado dentro de la familia denominada como Heptaxodontidae junto con otras tres especies Quemisia gravis (La Española), Xaymaca fulvopulvis (Jamaica) y Tainotherium valei (Puerto Rico). Sin embargo, las relaciones de estos roedores gigantes con los otros grupos de roedores caribeños ha sido tema de debate por décadas, particularmente porque no se ha llegado a un consenso respecto a cual de tres superfamilias principales de roedores caviomorfos pertenecen: Cavioidea, Chinchilloidea u Octodontoidea.
*Los roedores caribeños son tema recurrente en este blog, aquí los post pasados: los roedores más antiguos del Caribe (Parte 1, 2 y 3), los roedores endémicos que habitaban en Puerto Rico y el resumen de los resultados de un estudio sobre la microestructura de sus dientes.
El tema de la posición taxonómica de Heptaxodontidae se ha intensificado recientemente en gran parte por el descubrimiento de los roedores caviomorfos Borikenomys praecursor y una segunda especie más grande (aún sin nombrar), en depósitos del Oligoceno Temprano de Puerto Rico (Marivaux et al., 2020). Borikenomys comparte muchas características de sus molares con Elasmodontomys y Amblyrhiza. Cuando analizamos en detalle sus molares llegamos a la conclusión que esas especies forman parte de Chinchilloidea, lo cual sugiere: 1) que miembros de la superfamilia Chinchilloidea llegó a las Antillas mucho antes de lo previsto y, 2) que al menos algunos miembros de Heptaxodontidae son chinchilloideos (Marivaux et al., 2020). Estos resultados son similares a los de un estudio subsiguiente donde examinamos en detalle la microestructura de los incisivos de estos roedores (Marivaux et al., 2022). Sin embargo, en el tiempo transcurrido entre estas dos publicaciones, salió otro estudio con unos resultados interesantes, aunque contradictorios. Este otro trabajo por Roseina Woods y colegas analizan ADN antiguo (ADNa) obtenido de algunos de los roedores extintos del Caribe, incluyendo Elasmodontomys obliquus (Woods et al., 2021). Según sus resultados, Elasmodontomys, al igual que otras dos especies extintas, Brotomys voratus y Boromys offella (las cuales son parte del grupo de las ratas espinosas caribeñas [Heteropsomyinae]), ahora son parte de la familia Capromyidae, la cual incluye a las jutías que actualmente se pueden encontrar en algunas islas caribeñas. Basados en esos resultados, Woods et al. (2021) sugieren que todos los roedores caviomorfos endémicos de las Antillas pertenecen a una sola familia y representan un solo evento de colonización, en lugar de múltiples grupos y eventos como se ha propuesto en el pasado. Estos resultados contradicen los de nuestros estudios morfológicos para Elasmodontomys, al igual que otros estudios moleculares que incluyen a las jutías y ratas espinosas (e.g. Fabre et al., 2014; Courcelle et al., 2019; Marivaux et al., 2020, 2022). Desde mi punto de vista existen varias fallas en ese trabajo, desde un muestreo relativamente pequeño de las especies caribeñas extintas, a dudas sobre si el material que identificaron como Elasmodontomys y que usaron para el ADNa si representaba a esa especie y no a uno de los otros roedores que ocurren en el mismo depósito. Todo esto, en parte, nos trae al nuevo estudio.
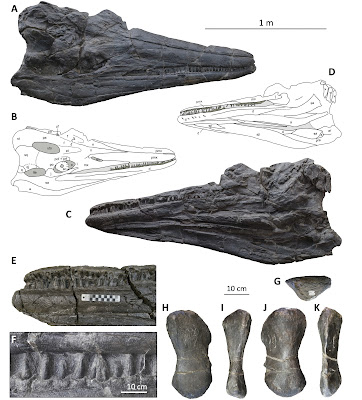
En este nuevo trabajo tomamos en cuenta una gran cantidad de especies extintas y actuales de roedores caribeños (Capromyinae, Heteropsomyinae y Heptaxodontidae), al igual que otros roedores, principalmente de América del Sur, con el fin de tener una representación de las todas las superfamilias de roedores caviomorfos (Erethizointoidea, Cavioidea, Chinchilloidea, Octodontoidea), para un total de 100 especies. Específicamente analizamos la morfología de la cóclea y los conductos semicirculares las cuales son las principales estructuras que se encuentran en el oído interno. La cóclea es la parte del oído interno que se encarga de la audición mientras que los conductos semicirculares (tres en total) se encargan del equilibrio. Para comparar las variaciones de la forma del oído interno entre las distintas especies utilizamos morfometría geométrica y métodos comparativos filogenéticos.
Los resultados más relevantes de este estudio es que demostramos que la morfología del oído interno tiene una señal filogenética fuerte, en otras palabras, que cada grupo muestra un patrón morfológico que los distingue de otros. Interesantemente, la morfología de lo oídos internos de Amblyrhiza inundata y Clidomys osborni sugieren que estos pertenecen dentro de Chinchilloidea, lo cual es congruente con nuestras observaciones morfológicas de los dientes. Sin embargo, Elasmodontomys obliquus continua siendo enigmático, ya que la morfología de su oído interno presenta afinidades con distintos grupos (Chinchilloidea ó Octodontoidea), dependiendo si los datos se analizan tomando en consideración cambios relacionados al tamaño de cuerpo o no (también conocido como alometría).
Aunque los resultados ambiguos para Elasmodontomys contradicen nuestros análisis (Marivaux et al., 2020, 2022), son más o menos consistente con los resultados de un estudio detallado de su basicráneo (MacPhee, 2011). Así que su relación con los otros roedores endémicos caribeños todavía no es clara, al menos por ahora. En otras palabras: ¡Elasmodontomys es raro!
Estas discrepancias morfológicas en Elasmodontomys puede que sean el resultado de algún efecto insular, o que quizás todavía no entendemos por completo los efectos de gigantismo y alometría en algunos grupos. Quizás en un futuro no tan distante se pueda replicar el estudio de ADN antiguo de Woods et al. (2021) o hacer estudios paleoproteómicos que nos ayuden a descifrar este misterioso roedor.
Literatura
Courcelle, M., M.-K. Tilak, Y. L. R. Leite, E. J. P. Douzeri, and P.-H. Fabre. 2019. Digging for the spiny rat and hutia phylogeny using a gene capture approach, with the description of new mammal subfamily. Molecular Phylogenetics and Evolution 136:241–253.
Da Cunha, L., L. W. Viñola-López, R. D. E. MacPhee, L. Kerber, J. Vélez-Juarbe, P.-O. Antoine, M. Boivin, L. Hautier, R. Lebrun, L. Marivaux, and P.-H. Fabre. 2023. The inner ear of caviomorph rodents: phylogenetic implications and application to extinct West Indian taxa. Journal of Mammalian Evolution. DOI: 10.1007/s10914-023-09675-3
Fabre, P.-H., J. T. Vilstrup, M. Raghavan, C. Der Sarkissian, E. Willerslev, E. J. P. Douzery, and L. Orlando. 2014. Rodents of the Caribbean: origin and diversification of hutias unravelled by next-generation museomics. Biology Letters 10:20140266.
MacPhee, R. D. E. 2011. Basicranial morphology and relationships of Antillean Heptaxodontidae (Rodentia, Ctenohystrica, Caviomorpha). Bulletin of the American Museum of Natural History 363:1–70.
Marivaux, L., L. W. Viñola-López, M. Boivin, L. Da Cunha, P.-H. Fabre, R. Joannes-Boyau, G. Maincent, P. Münch, N. S. Stutz, J. Vélez-Juarbe, and P.-O. Antoine. 2022. Incisor enamel microstructure of West Indian caviomorphs hystricognathous rodents (Octodontoidea and Chinchilloidea). Journal of Mammalian Evolution 29:969–995.
Marivaux, L., J. Vélez-Juarbe, G. Merzeraud, F. Pujos, L. W. Viñola-López, M. Boivin, H. Santos-Mercado, E. J. Cruz, A. Grajales, J. Padilla, K. I. Vélez-Rosado, M. Philippon, J.-L. Léticée, P. Münch, and P.-O. Antoine. 2020. Early Oligocene chinchilloid caviomorphs from Puerto Rico and the initial rodent colonization of the West indies. Proceedings of the Royal Society B 287:20192806.
Woods, R., I. Barnes, S. Brace, and S. T. Turvey. 2021. Ancient DNA suggest single colonization and within-archipelago diversification of Caribbean caviomorph rodents. Molecular Biology and Evolution 38:84–95.